2024 ESC Guidelines for the management of peripheral arterial and aortic diseases
Las guías clínicas publicadas recientemente por la Sociedad Europea de Cardiología (ESC) en 2024 aportan una orientación sobre el diagnóstico, tratamiento y seguimiento de las enfermedades arteriales y aórticas periféricas (PAAD).1 De hecho, son una actualización de las previas guías de práctica clínica de la ESC sobre enfermedad arterial periférica (EAP) incluyendo también en las actuales las enfermedades de la aorta con lo que ponen al día a la vez que hacen converger las guías de 2017 y 2014. Subrayan la importancia de adoptar una posición en la toma de decisiones compartida entre pacientes y médicos mediante la medición de resultados comunicados por el paciente (patient-reported outcome measures [PROM]) y la medición de la experiencia percibida por el paciente (patient-reported experience measures [PREM]), así como un enfoque multidisciplinario y sugiere el manejo de ciertas condiciones en centros especializados y de gran volumen de PAAD en cuanto a pacientes o procedimientos complejos. Las guías también destacan la necesidad de una evaluación integral de toda la circulación arterial en pacientes con PAAD (recomendación grado I, nivel de evidencia B).
Con respecto a la enfermedad arterial periférica (PAD o EAP; donde el término EAP se refiere a la enfermedad arterial aterosclerótica de las extremidades inferiores), se recomienda un enfoque no invasivo para el cribado inicial basado en el uso del índice tobillo-brazo (ITB) como primer escalón diagnóstico (Grado I/nivel B). Un ITB ≤0,9 se considera criterio diagnóstico para la EAP; sin embargo, encontramos a menudo un ITB ≥1,4 en pacientes con diabetes y/o enfermedad renal crónica debido a la presencia de calcificación de la media arterial. Por lo tanto, entre este subgrupo de pacientes se recomienda el uso de índices y técnicas alternativas como la presión parcial en el dedo del pie, el índice dedo-brazo o el análisis morfológico de la onda del Doppler (I/B).1
En estas guías se ha introducido una clasificación clínica de la EAP en tres grupos principales: EAP asintomática (generalmente identificada mediante exámenes de screening); EAP sintomática (ya relacionada con situaciones de esfuerzo); e isquemia crónica que amenaza la extremidad (CLTI), que incluye pacientes con dolor isquémico en reposo.
Se recomienda un enfoque terapéutico dirigido a diferentes dianas que incluya intervenciones no farmacológicas como cambios en el estilo de vida, asunción de una dieta saludable y práctica de actividad física, incluyendo bien programas de entrenamiento con ejercicios supervisados en el hospital o programas de ejercicio estructurados en el domicilio, así como intervenciones farmacológicas que incluyan medicamentos hipolipemiantes y/o antiplaquetarios y antitrombóticos. Con respecto a las intervenciones farmacológicas, las guías ESC 2024 recomiendan un tratamiento antiagregante plaquetario único con aspirina o clopidogrel en pacientes con EAP sintomática (I/A), y una pauta antitrombótica doble con dosis bajas de rivaroxabán y aspirina en pacientes con EAP con alto riesgo isquémico y bajo riesgo de sangrado (IIa/A).
Con respecto a las enfermedades aórticas, las guías ESC 2024 han introducido nuevos conceptos en el manejo de las dilataciones de la aorta ascendente como la inclusión de diversos parámetros más allá del diámetro aórtico para la indicación de cirugía, la importancia de evaluar el equilibrio entre el riesgo de eventos aórticos adversos y el riesgo quirúrgico y la homogeneidad de las indicaciones quirúrgicas tanto para la válvula aórtica tricúspide como para la bicúspide, aunque con diferentes niveles de recomendación.
Los factores de riesgo de rotura de un aneurisma de aorta toracoabdominal con válvula aórtica tricúspidea incluyen la hipertensión resistente no controlada, la tasa anual de crecimiento del diámetro aórtico, una longitud aórtica >11 mm, el diámetro aórtico indexado según la altura del paciente y el fenotipo aórtico de raíz, léase dilatación aórtica con diámetro sinusal > diámetro tubular versus dilatación aórtica ascendente. Tanto para la válvula aórtica tricúspide como para la bicúspide, la cirugía está indicada cuando el diámetro máximo de la aorta es de ≥55 mm (I/B). En el caso de las válvulas bicúspide, la cirugía está indicada para el fenotipo de raíz si el diámetro aórtico máximo es de ≥50 mm (I/B). En pacientes con bajo riesgo quirúrgico (<3%), se puede considerar el tratamiento quirúrgico para la dilatación aórtica ascendente >52 mm en la válvula aórtica tricúspide (IIa/B).
Con respecto a los síndromes aórticos agudos, las guías ESC 2024 han introducido una nueva clasificación: TEM, donde T representa el tipo de síndrome aórtico, E para la localización del desgarro de entrada y M para la presencia de mal perfusión, que conlleva implicaciones pronósticas y terapéuticas.
Se recomienda un algoritmo diagnóstico multiparamétrico que utilice un risk score para la detección de disección aórtica (I/B) que incluya la evaluación de factores predisponentes, características del dolor y signos de alto riesgo. Se aconseja la realización precoz de un angio-CT con contraste cérvico-toraco-abdomino-pélvico faseado con ECG como técnica de imagen de primera línea (I/C). Además, se recomienda el ecocardiograma transesofágico para orientar el manejo perioperatorio y detectar complicaciones tempranas (I/C). Para la disección aórtica aguda tipo B complicada con anatomía favorable para la reparación aórtica torácica endovascular, se recomienda la reparación endovascular (I/B), reservando la cirugía abierta como opción alternativa (I/B). Para la disección aórtica aguda tipo B sin complicaciones con anatomía favorable para la reparación aórtica endovascular torácica, se recomienda la reparación endovascular en la fase subaguda (IIa/B).
Desde el punto de vista del riesgo vascular, la presencia de EAP o enfermedad aórtica merece especial atención. Los pacientes con EAP tienen un alto riesgo de sufrir eventos adversos graves o mayores en las extremidades, incluida la revascularización y la amputación de estas, que en última instancia aumentan el riesgo de muerte.2 La EAP también se asocia con la enfermedad carotidea significativa y un mayor riesgo de eventos cardiovasculares adversos graves o importantes.3–5 Por lo tanto, los objetivos terapéuticos de la EAP incluyen mejorar la calidad de vida de los pacientes sintomáticos, reducir el riesgo de eventos adversos graves en las extremidades y disminuir el riesgo cardiovascular y cerebrovascular general.
Los aneurismas de aorta abdominal se asocian a una alta carga de riesgo vascular similar a la de la enfermedad polivascular, lo que conduce a un exceso de mortalidad en estos pacientes.6,7 Estudios previos han demostrado que los aneurismas de aorta torácica aislados tienden a tener un perfil de riesgo cardiovascular más bajo en comparación con los aneurismas de aorta abdominal.8 Un estudio de cohortes reciente en pacientes con edad avanzada sin accidente cerebrovascular previo encontró que las placas ateroscleróticas grandes (≥4 mm de grosor) en el arco aórtico se asociaron de forma independiente no solo con el accidente cerebrovascular sino con un resultado combinado de accidente cerebrovascular isquémico, infarto de miocardio y muerte cardiovascular (HR ajustado 2,19; IC 95 % [1,40–3,43]). Este hallazgo sugiere que las placas del arco aórtico pueden ser un marcador de riesgo cardiovascular más allá de una fuente directa de accidente cerebrovascular embólico.9
Las guías ESC 2024 introducen una nueva recomendación para iniciar el tratamiento con estatinas o el tratamiento antiagregante plaquetario único con clopidogrel o aspirina en dosis bajas en pacientes con placas de ateroma aórtica graves/complejas (IIa/C).
Dado el alto riesgo vascular de la mayoría de los pacientes con PAAD, el cribado de la enfermedad coronaria obstructiva (CAD) desempeña un papel crucial en la optimización del tratamiento médico y la planificación de estrategias de revascularización personalizadas.10
El uso del angio-CT coronario para la identificación de la CAD obstructiva se considera preciso en la mayoría de los pacientes con alto riesgo cardiovascular y supone una estrategia rápida y coste-efectiva para alcanzar un diagnóstico certero. La realización de la TC coronaria es sencilla desde el punto de vista operativo, ya que la mayoría de estos pacientes ya se someten a un angio-CT toracoabdominal con contraste como parte de la vía diagnóstica del PAAD.
En el caso de las intervenciones quirúrgicas urgentes, como la salvación aguda de una extremidad, la amputación de una extremidad o el tratamiento de la enfermedad aórtica aguda, el cribado de la enfermedad coronaria se aplaza imperiosamente; sin embargo, es necesario estar alerta de complicaciones cardiovasculares periprocedimiento. En el caso de las intervenciones quirúrgicas abiertas electivas, que tienden a conllevar un mayor riesgo de complicaciones cardiovasculares perioperatorias en comparación con las intervenciones endovasculares electivas, es deseable el cribado de la CAD antes de la intervención quirúrgica. Por lo tanto, está justificado un proceso de toma de decisiones compartido que involucre al paciente, así como a especialistas en PAAD, angiólogos, cirujanos vasculares, cardiólogos, cardiólogos intervencionistas y cirujanos cardíacos en casos de enfermedad multivaso y/o compleja. Este enfoque ayudará a definir un enfoque terapéutico personalizado con respecto al momento y la modalidad de intervención para la CAD obstructiva y la PAAD. El objetivo final es mejorar el resultado global de los pacientes y su calidad de vida, abordando las enfermedades clínicamente más relevantes de manera oportuna y eficaz.
Novedades en las recomendaciones en las enfermedades arteriales periféricas
Las enfermedades arteriales y aórticas periféricas PAAD son altamente prevalentes y aumentan significativamente la mortalidad y morbilidad cardiovascular en la población general, por lo que se requieren estrategias preventivas intensivas. Sin embargo, los pacientes con PAAD generalmente están infradiagnosticados e infratratados en comparación con los pacientes con enfermedad de las arterias coronarias. Estas guías clínicas de 2024 abordan conjuntamente la PAAD, actualizando y fusionando las directrices de enfermedades arteriales periféricas de 2017. Las nuevas directrices exploran las opciones de tratamiento, evalúan los valores de los pacientes y toman decisiones en colaboración con un enfoque multidisciplinario en centros expertos y de gran volumen de PAAD para pacientes o procedimientos complejos. Resaltamos las novedades relacionadas con el tratamiento médico del PAAD abordando las diferentes estrategias con respecto a las diferentes lesiones a tratar.
Manejo médico de la enfermedad arterial periférica
1 – Recomendaciones de terapia hipolipemiante
Los pacientes con enfermedad arterial periférica (EAP) sintomática tienen un riesgo vascular muy alto, pero generalmente se manejan de manera inadecuada en comparación con los pacientes con CAD. Se recomienda tanto la reducción del colesterol-LDL en un ≥50% de los valores basales como un objetivo de c-LDL de <1,4 mmol/L (<55 mg/dL) para disminuir el riesgo de muerte cardiovascular, infarto de miocardio y accidente cerebrovascular, así como para mejorar la distancia de claudicación (I/A). Las estatinas se recomiendan en todos los pacientes con EAP. Si no se alcanza el objetivo de colesterol LDL con estatinas y ezetimiba de máxima tolerancia, se recomienda el tratamiento con un inhibidor de PCSK9 para alcanzar los valores objetivo (I/A).
2 – Recomendaciones para el ejercicio físico
El entrenamiento con ejercicios supervisados (SET) se recomienda para pacientes con EAP sintomática y para pacientes después de la revascularización endovascular como terapia adyuvante (I/A). Se recomienda una intervención terapéutica con ejercicio supervisado con una frecuencia de entrenamiento al menos tres veces por semana con una duración de la sesión de al menos 30 minutos y duración del entrenamiento de al menos 3 meses antes de la toma de decisiones sobre la revascularización en el sector de la arteria femoral superficial (I/B).
3 – Recomendaciones para el tratamiento antitrombótico en pacientes con EAP
La aspirina (75-100 mg/día) para la prevención primaria puede considerarse en pacientes con EAP asintomática y diabetes, en ausencia de contraindicaciones (IIB/A). Se recomienda la estrategia antitrombótica simple con aspirina clopidogrel para la reducción de MACE en pacientes con EAP sintomática (I/A). Se debe considerar el tratamiento con pauta doble con combinación de 2,5 mg de rivaroxabán dos veces al día y aspirina (100 mg) en pacientes con EAP y alto riesgo isquémico con riesgo de hemorragia no alto (IIa/A) y en pacientes tras una revascularización de miembros inferiores (IIa/B).
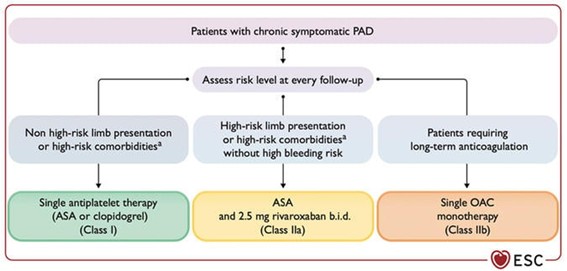
Fuente: European Heart Journal
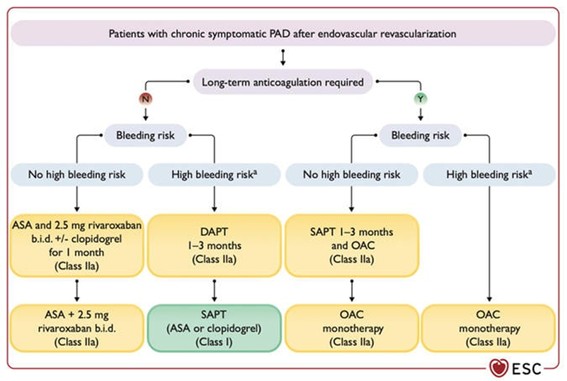
Fuente: European Heart Journal
4 – Recomendaciones para la imagen en pacientes con EAP
Se recomienda la ecografía dúplex como método de imagen de primera línea para confirmar las lesiones en la EAP (I/C). La valoración de las pruebas de imagen es crucial para correlacionar las lesiones con los síntomas, así como las pruebas hemodinámicas antes de indicar un procedimiento invasivo. Se recomienda el Angio-TAC y/o el angio-RM como técnicas adyuvantes para la planificación de las intervenciones de revascularización en la enfermedad aorto-ilíaca o de la enfermedad arterial compleja multisegmentaria (I/C).
Revascularización de miembros inferiores
1 – Revascularización en el sector aorto-ilíaco
Las lesiones aorto-ilíacas pueden tratarse mediante un abordaje endovascular o quirúrgico en función de la morfología de la lesión y el riesgo del paciente. Se consigue una permeabilidad a largo plazo razonable con un bajo riesgo de complicaciones mediante angioplastia con balón con o sin colocación de stent en las arterias ilíacas externas y con implante de stent primario en las arterias ilíacas comunes (IIa/B). En un metanálisis se evaluaron los resultados de la cirugía abierta frente a un abordaje endovascular en las lesiones aortoilíacas (TASC II C-D) y se encontró que la morbilidad y mortalidad a corto plazo favorece el abordaje endovascular, pero la permeabilidad primaria temprana y a medio plazo favorece la cirugía abierta. Sin embargo, la permeabilidad secundaria es comparable en todos los grupos.
2 – Revascularización en el sector femoro-poplíteo
En los casos en que la revascularización está indicada, el abordaje endovascular debe ser la primera opción (endo-first) incluso para lesiones complejas, especialmente en pacientes con alto riesgo quirúrgico. Los procedimientos endovasculares confrontan el desafío de mantener la permeabilidad y durabilidad a largo plazo en la región femoro-poplítea, particularmente tras la colocación de un stent en una arteria altamente móvil, como puede ser la arteria poplitea. Los balones liberadores de fármacos han mejorado la permeabilidad a largo plazo en cohortes de pacientes y lesiones complejas. Con respecto a los dispositivos recubiertos con paclitaxel, la FDA restringió temporalmente su uso tras un recall debido a los resultados de un metaanálisis que recogían un aumento en la mortalidad entre los pacientes que fueron tratados con esta modalidad. Subsiguientemente, se analizaron los datos de grandes bases de datos nacionales y pudiendose confirmar tal aumento en la mortalidad. La FDA revisó su posición, y ahora se considera que los procedimientos con liberación de fármacos es una estrategia de tratamiento segura y eficiente para las lesiones femoro-poplíteas.
En las lesiones femoro-poplíteas, el tratamiento con liberación de fármacos debe considerarse como la estrategia de primera elección (IIa/A).
Debe considerarse un abordaje quirúrgico abierto en las lesiones femoro-poplíteas cuando se dispone de una vena autóloga de calidad (p. ej., vena safena interna) si el paciente aporta un riesgo quirúrgico bajo, y en lesiones complejas tomando en cuenta las particularidades específicas del caso habiendo sido discutido en sesión clínica interdisciplinar.
3 – Revascularización en el sector infragenicular
En lesiones infrapoplíteas cortas, el tratamiento endovascular es de primera elección (endo-first). Los balones liberadores de fármacos y el implante de stents no recubiertos no han mostrado superioridad sobre la angioplastia simple con balón, aunque los stents liberadores de fármacos pueden utilizarse para lesiones proximales relativamente cortas.
4 – Isquemia crítica de las extremidades (CLI)
Para los pacientes con CLI, se recomienda realizar la revascularización lo antes posible (I/B). Es necesaria una valoración individual del riesgo por parte de un equipo vascular multidisciplinario para elegir la revascularización endovascular frente a la quirúrgica abierta (I/C). Si el paciente necesita cirugía abierta por lesiones femoropoplíteas, se recomiendan venas autólogas (I/B). En los pacientes con CLI, el tratamiento endovascular puede considerarse como terapia de primera línea, especialmente en pacientes con mayor riesgo quirúrgico o venas autólogas inadecuadas (IIb/B).
Estenosis de la arteria carótida extracraneal y estenosis de la arteria subclavia
En función a los estudios recientes sobre el manejo de la estenosis de la arteria carótida extracraneal comparando el tratamiento endovascular, la endarterectomía y la terapia médica óptima, las guías de la ESC 2024 brindan un algoritmo para pacientes asintomáticos y sintomáticos:
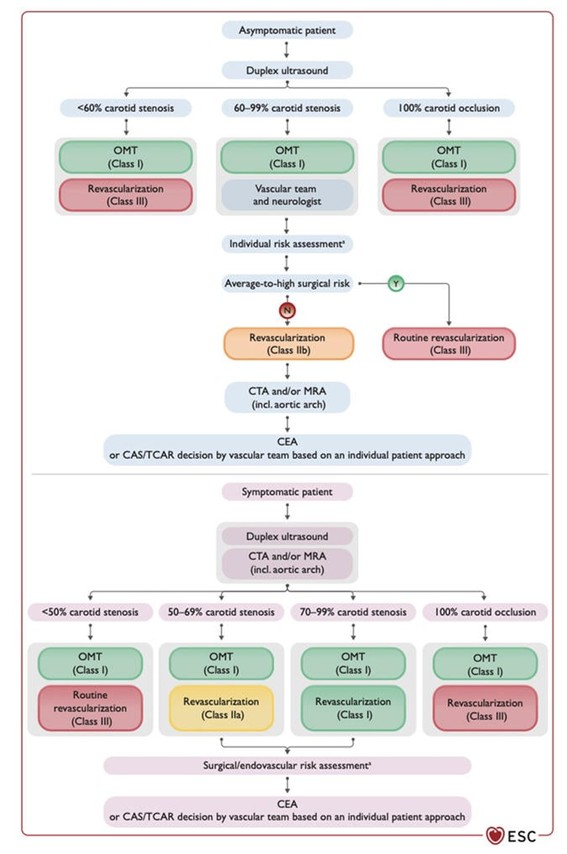
Fuente: European Heart Journal
En cuanto a la estenosis de la arteria subclavia asintomática, no hay lugar para la revascularización rutinaria. Se podría considerar el tratamiento solo en caso de bypass mamario-coronario (IIa/C).
Estenosis de la arteria renal
Se recomienda la ecografía dúplex como modalidad de imagen de primera línea en pacientes con sospecha de estenosis de la arteria renal (RAS) (I/B). En pacientes con RAS aterosclerótico unilateral o bilateral > 70% con signos de viabilidad renal, se debe considerar la revascularización de la arteria renal secundariamente a un tratamiento médico óptimo (IIa/B). Se resume un algoritmo para el diagnóstico y el tratamiento de RAS.
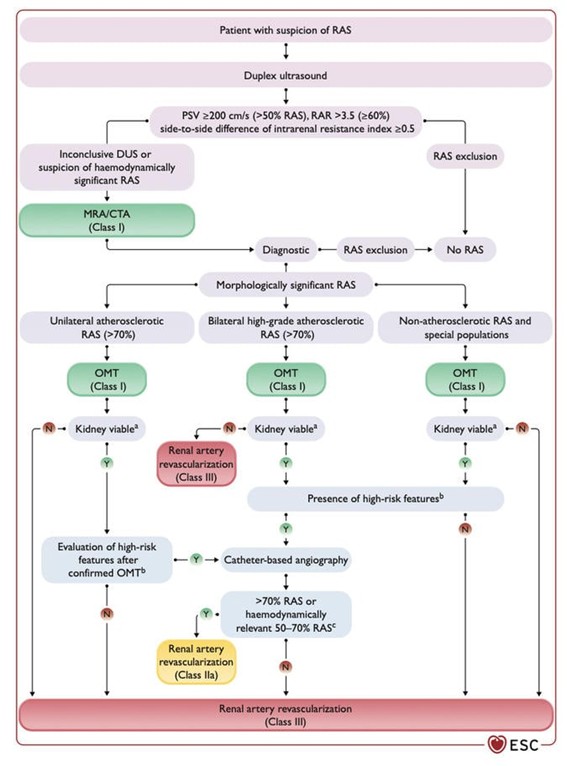
Fuente: European Heart Journal
Referencias
- Mazzolai L, Teixido-Tura G, Lanzi S, et al. 2024 ESC Guidelines for the management of peripheral arterial and aortic diseases. Eur Heart J 2024;45:3538–700.
- Anand SS, Caron F, Eikelboom JW, et al. Major adverse limb events and mortality in patients with peripheral artery disease. J Am Coll Cardiol 2018;71:2306–15.
- Ramos MJ, González-Fajardo JA, Vaquero-Puerta C, et al. Asymptomatic carotid stenosis in patients with intermittent claudication: epidemiological study. J Cardiovasc Surg (Torino) 2011;52:761–8.
- Hageman SHJ, de Borst GJ, Dorresteijn JAN, et al. Cardiovascular risk factors and the risk of major adverse limb events in patients with symptomatic cardiovascular disease. Heart 2020;106:1686–92.
- Eikelboom JW, Connolly SJ, Bosch J, et al. Rivaroxaban with or without aspirin in stable cardiovascular disease. N Engl J Med 2017;377:1319–30.
- Kaasenbrood L, Boekholdt SM, van der Graaf Y, et al. Distribution of estimated 10-year risk of recurrent vascular events and residual risk in a secondary prevention population. Circulation 2016;134:1419–29.
- Bulder RMA, Talvitie M, Bastiaannet E, et al. Long-term prognosis after elective abdominal aortic aneurysm repair is poor in women and men: the challenges remain. Ann Surg 2020;272:773–8.
- Dolmaci OB, El Mathari S, Driessen AHG, et al. Are thoracic aortic aneurysm patients at increased risk for cardiovascular diseases? J Clin Med 2022;12:272.
- Yoshida Y, Jin Z, Mannina C, et al. Aortic arch plaques and the long-term risk of stroke and cardiovascular events in the statin era. Stroke 2024;55:69–77.
- Halvorsen S, Mehilli J, Cassese S, et al. 2022 ESC Guidelines on cardiovascular assessment and management of patients undergoing non-cardiac surgery. Eur Heart J 2022;43:3826–924.
Dr. Joaquín de Haro Miralles

Angiología y Cirugía Vascular.
Hospital Universitario Getafe, Madrid.


